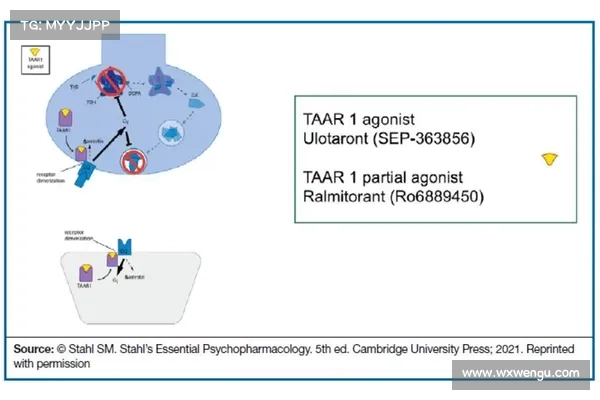
本文将详细探讨TAAR1(胺类受体1型)与5-HT2CR(5-羟色胺2C型受体)药物的临床试验流程与实施步骤。随着精神疾病、神经系统疾病等多种疾病的治疗需求不断增加,相关药物的临床试验流程尤为关键。通过对TAAR1与5-HT2CR药物临床试验的流程、实施步骤以及挑战进行详细阐述,本文旨在为研究人员提供一种清晰的框架,帮助更好地理解这些药物的临床开发路径。文章将从试验设计、伦理审查、患者招募、临床监控等四个方面详细分析药物试验的实施流程,为相关领域的专业人员提供实用的参考。
1、临床试验设计的基础
临床试验设计是药物研发过程中最为关键的步骤之一,直接决定了试验的有效性与可靠性。在TAAR1和5-HT2CR药物的临床试验中,首先需要根据药物的作用机制、预期疗效以及适应症的不同,确定试验的总体设计框架。通常包括临床前研究、I期、II期和III期等不同阶段,每一阶段的设计要求和目标不同。例如,I期试验主要关注药物的安全性,II期则侧重于药物的疗效评估,III期则是大规模样本的验证试验。
在TAAR1和5-HT2CR的临床试验中,研究人员需要特别注意受试者的选择标准。受试者的筛选不仅仅依赖于病理诊断,还需要考虑个体差异,例如基因型、药物代谢情况等生物标志物。这一过程对于确保临床试验的科学性和有效性至关重要。同时,试验的设计还要考虑到对照组的设置,通常会设立安慰剂组或现有治疗方法的对照组,确保能够有效对比新药与现有治疗方法的疗效差异。
此外,试验设计还需要详细规划每个试验阶段的时间节点、样本量、数据收集与分析方法等。这些因素都会直接影响到临床试验的进度、结果的可信度以及药物的上市时间。因此,精确而合理的试验设计为药物的最终成功上市打下了坚实的基础。
2、伦理审查与临床试验批准
伦理审查是每一项临床试验开展前的必经环节,确保试验过程中受试者的权益得到最大程度的保障。TAAR1和5-HT2CR药物的临床试验在开展前,必须通过伦理委员会的审查。伦理委员会主要负责评估试验设计的合理性,确保试验方案符合伦理要求,并对试验中可能出现的风险进行预估与规避。
临床试验的伦理审查内容包括:首先,研究者需提交详细的试验方案,方案中必须包括研究目的、试验方法、患者选择标准、药物剂量、给药方案、副作用监测等;其次,试验需要明确告知受试者可能面临的风险,包括药物可能的副作用以及其他不良反应;最后,受试者是否能够自主选择是否参与,是否有足够的知情同意,所有这些都是伦理审查的重要部分。
除了伦理委员会的审查,临床试验还需要得到相关药品监管机构的批准。在中国,药物的临床试验需要获得国家药品监督管理局(NMPA)的批准;在美国,则需通过FDA(美国食品药品监督管理局)审批。监管机构会依据临床试验的设计、数据和安全评估报告,对药物是否进入下一阶段的试验进行审批。这一过程确保了药物试验的合法性和合规性。
3、患者招募与知情同意
患者招募是临床试验中最为繁琐且至关重要的环节之一。TAAR1和5-HT2CR药物的临床试验往往涉及大量患者的招募,这需要研究人员通过多种途径进行宣传与招募。常见的招募方式包括在医院内外的广告、线上平台招募、社交媒体宣传等。为了确保招募的患者符合试验要求,招募过程中必须进行严格筛选。
患者招募时,研究人员首先要确保受试者符合试验的纳入标准,这些标准通常包括疾病类型、病程、年龄、性别等因素。与此同时,受试者还必须排除那些可能因其他疾病或特殊生理状态(如孕妇)而不适合参加试验的个体。患者筛选不仅要确保试验结果的科学性,还要保护患者的健康,防止因不合适的患者进入试验组而造成的安全隐患。
在患者成功招募后,接下来是知情同意的环节。研究人员需要对患者进行详细的药物作用、试验流程、可能的风险与副作用等方面的解释,确保患者完全理解后自愿参与试验。知情同意书必须包括患者的个人信息、试验的目标、方法、潜在风险、受益等内容,并且患者需要签字确认。这个过程对保护患者的合法权益至关重要,同时也是临床试验能够顺利进行的前提。
4、临床监控与数据管理
临床试验的监控与数据管理是确保试验质量和试验结果可靠性的关键环节。在TAAR1与5-HT2CR药物的临床试验中,数据的准确性、完整性和时效性至关重要。研究团队通常会指派专门的临床监控员(CRA)负责日常监控工作。监控员需要定期对试验过程中的数据进行审核,确保每个环节按照标准操作程序(SOP)执行,发现问题及时修正。
临床监控员的职责包括:第一,确保药物的剂量、给药方法、试验记录等符合预定方案;第二,及时发现并报告受试者的不良反应和副作用,确保患者的安全;第三,确保所有的试验数据都得到了正确记录,并且数据的保密性得到了保障。监控员与临床研究团队密切合作,保证临床试验的顺利推进。
另外,数据管理的工作同样不可忽视。临床试验过程中收集的数据通常为大量且复杂,必须采用专业的电子数据采集系统(EDC)进行存储和分析。数据管理人员需要确保所有数据的准确录入、存档与处理,并且确保数据的安全性与合规性。在试验结束后,研究人员会对数据进行统计分析,判断药物的安全性与有效性。这些数据将成为临床报告的核心内容,直接影响药物的批准与上市。
总结:
本文从试验设计、伦理审查、患者招募、临床监控四个方面详细阐述了TAAR1与5-HT2CR药物的临床试验流程与实施步骤。临床试验作为药物研发的重要环节,涉及多个复杂的步骤,每一步都要求严谨与科学。在试验设计方面,合理的设计框架、合适的患者筛选标准以及科学的对照组设置是药物临床试验成功的基础;而伦理审查则保证了患者的安全与试验的合法性;患者招募与知情同意程序则是保证研究对象权益的重要手段;最后,临床监控与数据管理确保了药物试验的质量与可信度。
随着TAAR1与5-HT2CR药物临床试验的不断深入,未来的临床研究将在更大范围内探索其治疗潜力。这些药物不仅有望为精神疾病和神经系统疾病的治疗提供新选择,也为相关药物的研发提供了宝贵的经验与教训。未来,随着技术的进步与伦理标准的提升,药物临床试验将更加高效、透明,最终推动更多创新药物的上市。
九游会(J9)官方网站-真人游戏第一品牌[VIP]![九游会(J9)官方网站-真人游戏第一品牌[VIP]](https://www.wxwengu.com/upload/image/jiu-you-hui-J9-guan-fang-wang-zhan-zhen-ren-you-xi-di-yi-pin-pai-logo.webp)